
Secciones
Servicios
Destacamos

La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha retirado un lote de test autodiagnóstico de la covid-19 fabricados en China tras varios avisos de usuarios detectando problemas en su funcionamiento.
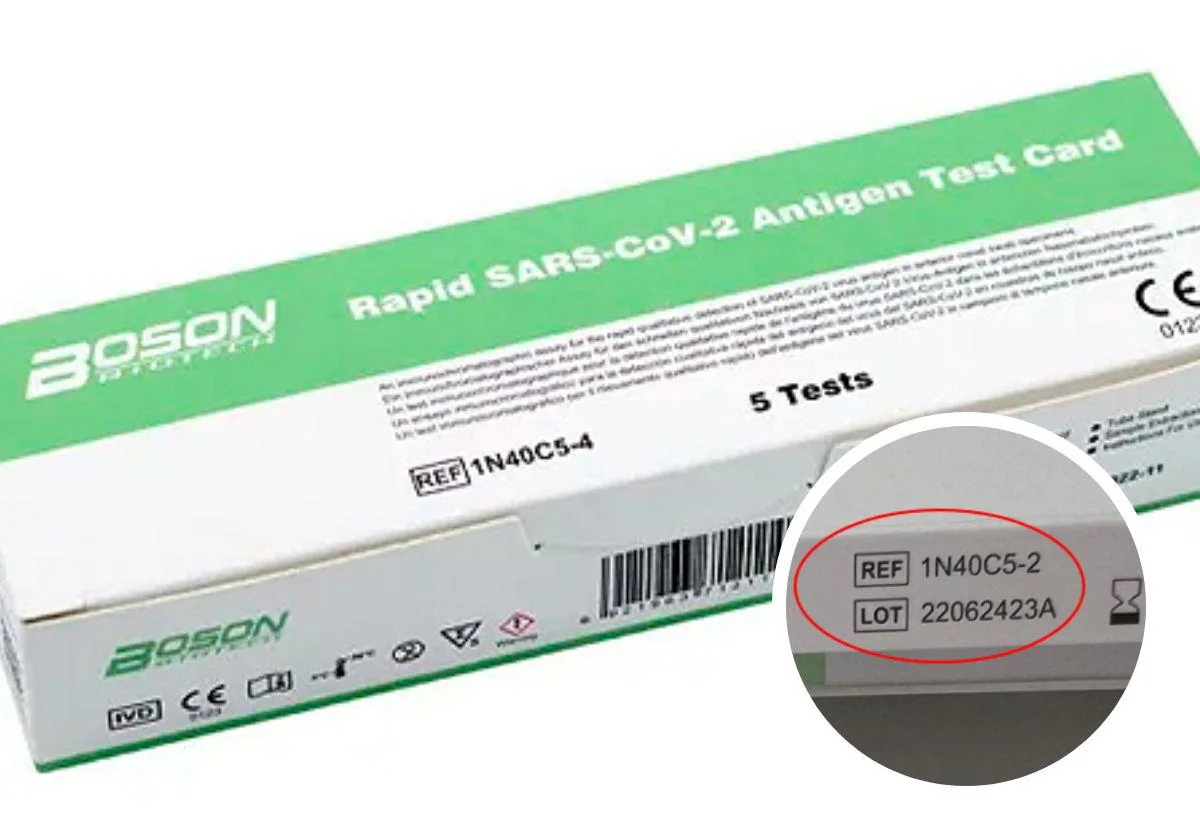
El producto afectado se ha producido en los test rápidos de antígenos para autodiagnóstico de la COVID-19 Rapid SARS-CoV-2 Antigen Test Card, fabricados por el laboratorio chino Xiamen Boson Biotech en el lote con referencia 1N40C5-2.
En concreto, el fallo comunicado se produce en el líquido reactivo que contienen estos test, llamado buffer, que se evapora total o parcialmente antes del uso. Este error provoca que la prueba se complete de manera correcta al no disponer de una cantidad suficiente de buffer, dando lugar a resultados incorrectos o pruebas nulas.
La AEMPS, al recibir numerosas comunicaciones sobre esa situación en estos test rápidos de antígenos, inició de forma inmediata una investigación en la que se puso en contacto con el fabricante de los productos para conocer la causa, así como la trazabilidad, distribución y situación de estos productos en el mercado español.
Noticias relacionadas
El laboratorio chino ha identificado un problema en el sellado de los buffers y ha adoptado las medidas correctivas para solucionar el problema a partir del número de lote 22122707A, por lo que todos los lotes con numeración anterior al indicado pueden verse afectados.
Por ello, desde la Agencia Española de Medicamentos y Productos Santiarios se ha solicitado el cese voluntario de la comercialización y retirada de los lotes con número anterior al 22122707A tanto al fabricante como a los distribuidores identificados, incluidas las oficinas de farmacia de España que dispongan de unidades de Rapid SARS-CoV-2 Antigen Test Card, fabricado por Xiamen Boson Biotech Co, Ltd, China con referencia 1N40C5-2 y con número de lote anterior al 22172707A.
A estas, la AEMPS les ha urgido a tomar las medidas adecuadas para evitar su utilización, recomendaciones que instan a las farmacias del país a examinar sus registros de trazabilidad, comprobar si se dispone de estas unidades para evitar su distribución, retirarlas de la venta y devolveras al proveedor.
Respecto a los usuarios que pudiesen haberlas adquirido, la agencia explica que se debe comprobar la referencia y el lote y en caso afirmativo, dejar de utilizarlo de inmediato y poner el incidente en conocimiento de las autoridades pertinentes a través del portal NotificaPS.
Publicidad
Publicidad
Te puede interesar
Publicidad
Publicidad
Esta funcionalidad es exclusiva para registrados.
Reporta un error en esta noticia

Debido a un error no hemos podido dar de alta tu suscripción.
Por favor, ponte en contacto con Atención al Cliente.

¡Bienvenido a BURGOSCONECTA!

Tu suscripción con Google se ha realizado correctamente, pero ya tenías otra suscripción activa en BURGOSCONECTA.
Déjanos tus datos y nos pondremos en contacto contigo para analizar tu caso

¡Tu suscripción con Google se ha realizado correctamente!
La compra se ha asociado al siguiente email
Comentar es una ventaja exclusiva para registrados
¿Ya eres registrado?
Inicia sesiónNecesitas ser suscriptor para poder votar.